La nueva era de la medicina estética regenerativa
La medicina estética moderna se aleja de los tratamientos basados exclusivamente en relleno o corrección inmediata para avanzar hacia terapias regenerativas, cuyo propósito es restaurar la biología del tejido, reprogramar el microambiente dérmico y modular vías celulares específicas.
En este contexto, los Polinucleótidos (PN) y el Polidesoxirribonucleótido (PDRN) derivados del ADN de salmón se han consolidado como herramientas altamente seguras y científicamente respaldadas, con evidencia creciente en reparación tisular, modulación inflamatoria, angiogénesis y regulación pigmentaria.
1 ¿Qué son los PN y el PDRN?
1.1 Polinucleótidos (PN) — macromoléculas regenerativas
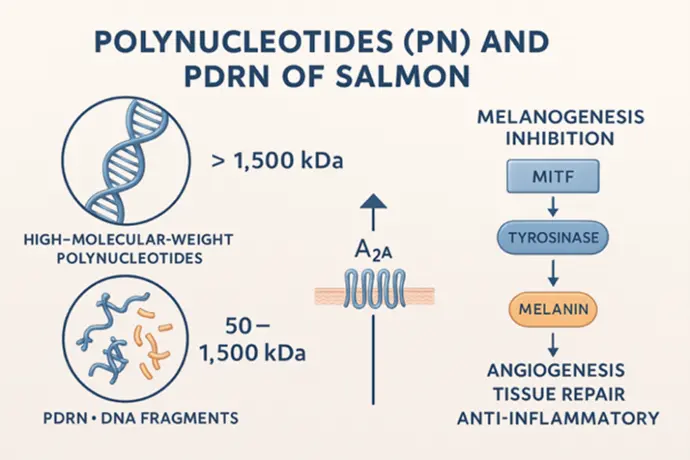
Los PN son fragmentos altamente purificados de ADN de salmón, con un peso molecular superior a 1 500 kDa, lo que les confiere:
- elevada viscoelasticidad,
- capacidad de retención hídrica,
- fuerte actividad antioxidante,
- propiedades de reorganización dérmica,
- y efectos moduladores en melanogénesis.
Su tamaño molecular explica su acción predominantemente extracelular, actuando como biomaterial bioactivo capaz de influir en el microambiente dérmico.
1.2 PDRN — fracción bioactiva de menor peso molecular
El PDRN consiste en fragmentos de ADN con un peso molecular entre 50 y 1 500 kDa, con predominio en la fracción baja del espectro (50–150 kDa).
Este menor tamaño le permite:
- interactuar más eficientemente con el receptor A2A,
- modular vías inflamatorias,
- promover angiogénesis,
- y acelerar reparación tisular.
PN y PDRN no son intercambiables: sus efectos, dianas biológicas e indicaciones son distintas.
2 Mecanismos de acción basados en evidencia
2.1 Activación del receptor A2A — predominante en PDRN
La activación del receptor adenosina A2A conduce a:
↑ VEGF → angiogénesis,
↑ TGF-β → reparación tisular,
↓ TNF-α y ↓ IL-6 → efecto antiinflamatorio,
↑ actividad fibroblástica,
↑ remodelación de colágeno.
El PDRN es el agonista más potente sobre esta vía debido a su menor tamaño molecular.
2.2 Modulación de la matriz extracelular — predominante en PN
Los PN, por su macroestructura (>1 500 kDa), actúan como un andamio biológico, capaz de:
- mejorar hidratación intersticial profunda,
- reorganizar fibras de colágeno y elastina,
- disminuir degradación por MMP-1 y MMP-3,
- reducir daño oxidativo,
- y mejorar la biomecánica de la piel.
Este mecanismo los hace ideales para el fotoenvejecimiento y la pérdida de calidad dérmica.
2.3 Modulación de la melanogénesis: PN y la vía de tirosinasa/MITF
Uno de los hallazgos más relevantes en investigación reciente es la capacidad de los PN para regular directamente la producción de melanina, a través de mecanismos moleculares precisos:
- Inhibición de tirosinasa (Tyr) enzima clave en la conversión de tirosina a L-DOPA disminuye la síntesis de melanina.
- Regulación de MITF (Microphthalmia-associated Transcription Factor) Factor maestro que regula todos los genes melanogénicos menor expresión de Tyr, TRP-1 y TRP-2.
- Reducción de ROS : menor estrés oxidativo menor estímulo para melanogénesis UV e inflamatoria.
Estos efectos hacen del PN una herramienta ideal para:
- melasma,
- hiperpigmentación post-inflamatoria (PIH),
- ojeras pigmentadas,
- rejuvenecimiento periocular.
3 Evidencia clínica reciente
Varios estudios clínicos han demostrado:
- ↑ grosor dérmico medido por ultrasonido,
- ↑ elasticidad (Cutometer),
- disminución de arrugas finas perioculares,
- reducción significativa de melasma y PIH,
- mejora notable en luminosidad y uniformidad,
- aceleración en la epitelización post-láser,
- disminución del eritema post-procedimiento.
Las mejoras más consistentes se observan tras 2–3 sesiones, dependiendo del tipo de piel y protocolo.
4 Indicaciones clínicas principales
4.1 Indicaciones de PN (>1 500 kDa)
-
- Melasma e hiperpigmentación
- Envejecimiento periocular
- Piel fina y fotoenvejecida
- Fotoenvejecimiento cervical y dorsal
- Calidades dérmicas irregulares
- Luminosidad y biorevitalización global
4.2 Indicaciones de PDRN (50–1 500 kDa)
-
- Rosácea inflamatoria
- Piel sensibilizada o reactiva
- Recuperación post-láser CO₂ / Er:YAG
- Inflamación crónica
- Cicatrización post-procedimientos
- Reparación acelerada en piel dañada
5 Perfil de seguridad
PN y PDRN son:
- no particulados,
- no proinflamatorios,
- con riesgo virtualmente nulo de granulomas,
- seguros en todos los fototipos,
- adecuados para piel sensible o reactiva,
- compatibles con la mayoría de las terapias regenerativas,
- de los productos con mejor perfil de seguridad en estética médica.
Conclusión Dr to Dr Academy
Los Polinucleótidos (PN) y el PDRN no son simples biorevitalizantes: son verdaderas herramientas regenerativas respaldadas por biología molecular y evidencia clínica.
Los PN destacan en arquitectura dérmica, hidratación profunda y despigmentación, mientras que el PDRN sobresale en antiinflamación, reparación tisular y angiogénesis.
Su perfil de seguridad, sumado a su acción regenerativa real, los posiciona como una de las terapias más consistentes para la piel en 2025.
Bibliografía indexada (2020–2025)
- Park H et al. Polynucleotides suppress UV-induced melanogenesis via MITF/Tyr downregulation. Int J Mol Sci. 2024.
- Kim MJ et al. Antioxidant and anti-melanogenic properties of high–molecular-weight salmon DNA PN. J Cosmet Dermatol. 2023.
- Lee Y et al. Differential molecular pathways of PN vs PDRN in melanogenesis and inflammation. Dermatol Ther. 2022.
- Gu SY et al. PDRN accelerates post-laser wound healing through A2A receptor activation. Lasers Med Sci. 2024.
- Shin JW et al. Dermal thickness and elasticity improvements after PN injections in periocular tissue. Aesthetic Surg J. 2022.
- Hong K et al. Safety of salmon-derived polynucleotides in regenerative dermatology. J Dermatolog Treat. 2022.
- Kim JH et al. A2A receptor-driven anti-inflammatory and angiogenic effects of PDRN. Int J Mol Sci. 2023.
- Amore E et al. Tissue repair and anti-inflammatory actions of PDRN. Pharmacol Res. 2020.
- Byun K et al. PN enhances extracellular matrix architecture and reduces oxidative stress in aged skin. Skin Res Technol. 2021.